Phân tử, nguyên tử, electron, proton, nơtron – những khái niệm tưởng chừng khô khan nhưng lại là nền tảng cho thế giới hóa học đầy màu sắc. Bài 12 trong Sách Bài Tập Hóa Học 8 sẽ dẫn dắt chúng ta tìm hiểu về sự chuẩn bị dung dịch, một kỹ năng quan trọng trong phòng thí nghiệm và cả trong cuộc sống hàng ngày.
Khái Niệm Dung Dịch và Nồng Độ Dung Dịch
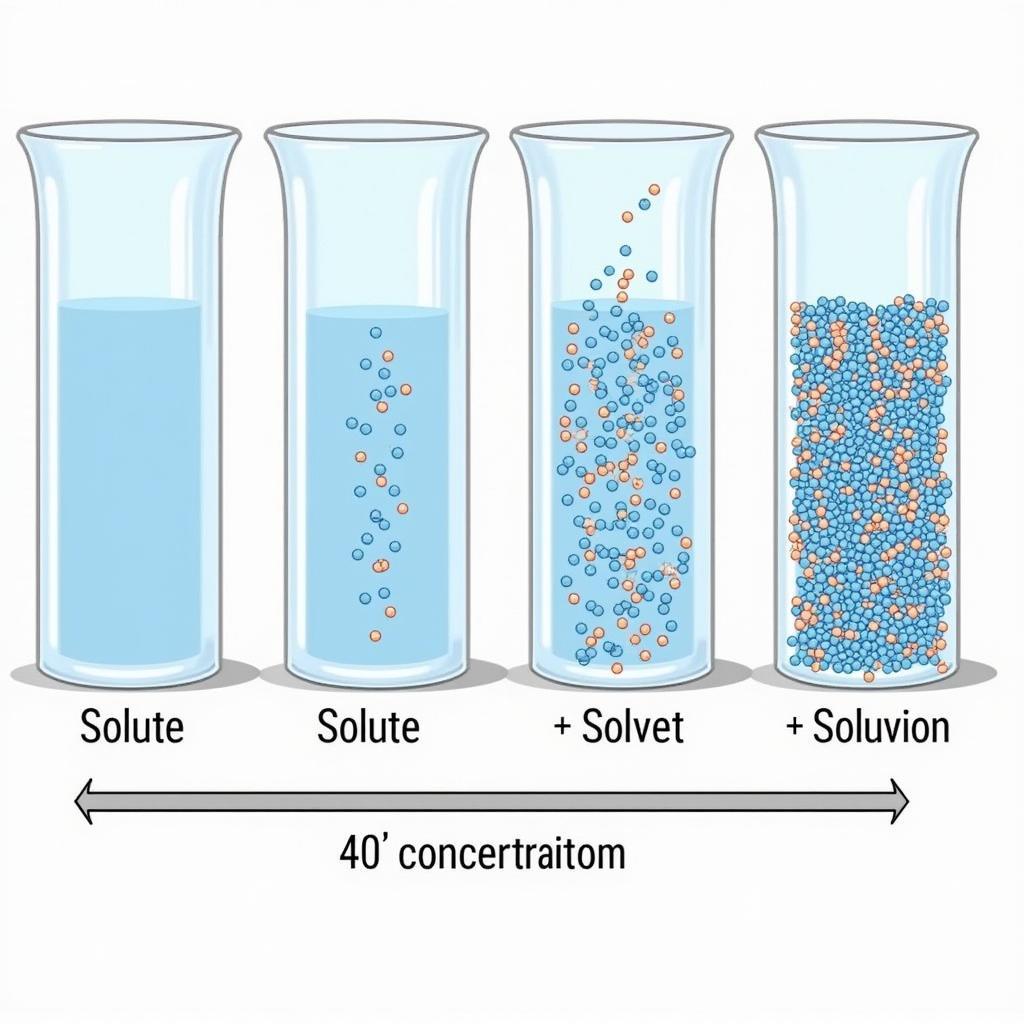
Dung dịch là một hỗn hợp đồng nhất gồm chất tan và dung môi. Chất tan là chất được hòa tan trong dung môi. Dung môi thường là chất lỏng, ví dụ như nước. Nồng độ dung dịch thể hiện lượng chất tan có trong một lượng dung dịch nhất định. Nồng độ phần trăm (C%) là một cách phổ biến để biểu thị nồng độ, được tính bằng khối lượng chất tan chia cho khối lượng dung dịch, nhân với 100%.
Cách Pha Chế Dung Dịch
Để pha chế một dung dịch có nồng độ phần trăm xác định, ta cần tính toán khối lượng chất tan và khối lượng dung môi cần dùng. Công thức tính khối lượng chất tan (mct) là mct = (C% * mdd) / 100%, trong đó mdd là khối lượng dung dịch. Khối lượng dung môi (mdm) được tính bằng mdd – mct.
Ví dụ, để pha chế 200g dung dịch NaCl 10%, ta cần (10% * 200g) / 100% = 20g NaCl và 200g – 20g = 180g nước. Đầu tiên, cân chính xác 20g NaCl. Sau đó, hòa tan NaCl vào 180g nước trong một bình định mức. Khuấy đều cho đến khi NaCl tan hoàn toàn. Bạn có thể tham khảo thêm về các bài tập vật lý tại giải bài tập lý 8 bài 9.
Bài Tập Áp Dụng
Sách Bài Tập Hóa Học 8 cung cấp nhiều bài tập giúp học sinh rèn luyện kỹ năng tính toán và pha chế dung dịch. Các bài tập này bao gồm tính nồng độ phần trăm, tính khối lượng chất tan, khối lượng dung môi, và pha chế dung dịch theo nồng độ cho trước.
“Việc luyện tập thường xuyên các bài tập là chìa khóa để nắm vững kiến thức về dung dịch,” Ông Nguyễn Văn A, giáo viên hóa học với 15 năm kinh nghiệm chia sẻ. “Học sinh nên bắt đầu từ những bài tập cơ bản rồi nâng cao dần độ khó.”
Kết Luận
Giải SBT Hóa 8 Bài 12 cung cấp kiến thức nền tảng về dung dịch và nồng độ dung dịch, cùng với các phương pháp pha chế dung dịch. Việc hiểu rõ những khái niệm này không chỉ giúp học sinh đạt điểm cao trong các bài kiểm tra mà còn có ứng dụng rộng rãi trong cuộc sống. Tìm hiểu thêm về các giải đáp khác tại giải sách bài tập hóa học 8.
FAQ
- Dung dịch là gì?
- Nồng độ phần trăm là gì?
- Cách tính khối lượng chất tan?
- Cách pha chế dung dịch NaCl 10%?
- Tại sao cần học về dung dịch?
- Tôi có thể tìm thấy bài tập về dung dịch ở đâu?
- Làm thế nào để tính khối lượng dung môi?
Bạn cũng có thể tìm hiểu thêm về giải vật lý 9 bài 35 hoặc giải địa lý 9 bài 27. giải tiếng anh lớp 9 unit 2 skills 2 cũng là một lựa chọn thú vị.
Khi cần hỗ trợ hãy liên hệ Số Điện Thoại: 0372999996, Email: bong.da@gmail.com Hoặc đến địa chỉ: 236 Cầu Giấy, Hà Nội. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.