Điều chế kim loại là một quá trình quan trọng trong hóa học, biến đổi các hợp chất kim loại thành dạng kim loại tinh khiết. Giải bài tập điều chế kim loại không chỉ giúp học sinh nắm vững kiến thức lý thuyết mà còn rèn luyện kỹ năng phân tích và giải quyết vấn đề. Bài viết này sẽ cung cấp cho bạn những phương pháp và ví dụ cụ thể để giải quyết các dạng bài tập điều chế kim loại thường gặp.
Sau khi tìm hiểu về màng não giải phẫu, chúng ta cùng đi sâu vào nội dung chính.
Các Phương Pháp Điều Chế Kim Loại
Có nhiều phương pháp điều chế kim loại khác nhau, tùy thuộc vào bản chất của kim loại và hợp chất của nó. Một số phương pháp phổ biến bao gồm:
- Nhiệt luyện: Sử dụng nhiệt độ cao để khử oxit kim loại bằng các chất khử như cacbon, CO, hoặc hydro. Phương pháp này thường áp dụng cho các kim loại có tính khử trung bình và yếu.
- Thủy luyện: Sử dụng dung dịch để tách kim loại ra khỏi quặng. Phương pháp này thường được sử dụng cho các kim loại có tính khử mạnh.
- Điện phân: Sử dụng dòng điện để khử ion kim loại trong dung dịch hoặc muối nóng chảy. Phương pháp này thường được sử dụng để điều chế các kim loại có tính khử mạnh và rất mạnh.
Hướng Dẫn Giải Bài Tập Điều Chế Kim Loại Bằng Phương Pháp Nhiệt Luyện
- Xác định chất tham gia: Xác định oxit kim loại cần điều chế và chất khử được sử dụng.
- Viết phương trình phản ứng: Viết phương trình phản ứng nhiệt luyện, cân bằng phương trình.
- Tính toán số mol: Tính toán số mol của các chất tham gia dựa trên khối lượng hoặc thể tích cho trước.
- Xác định chất dư/thiếu: Xác định chất nào là chất dư, chất nào là chất thiếu dựa trên tỉ lệ mol trong phương trình phản ứng.
- Tính toán khối lượng kim loại: Tính toán khối lượng kim loại được điều chế dựa trên số mol của chất thiếu.
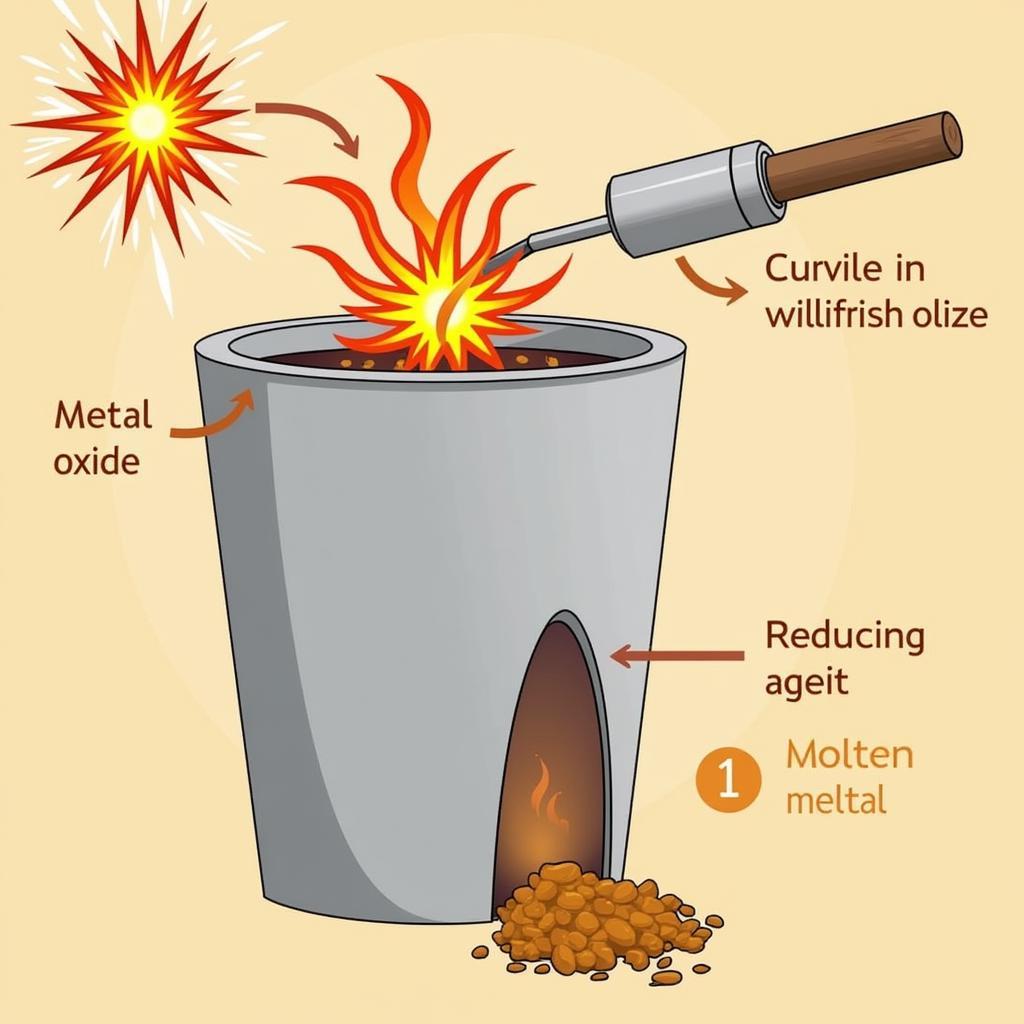 Giải bài tập điều chế kim loại bằng phương pháp nhiệt luyện
Giải bài tập điều chế kim loại bằng phương pháp nhiệt luyện
Giải Bài Tập Điều Chế Kim Loại Bằng Phương Pháp Thủy Luyện
Quá trình thủy luyện thường được ứng dụng trong việc tách kim loại ra khỏi quặng. Tìm hiểu thêm về giải bài tập hóa 9 một số muối quan trọng.
- Xác định phản ứng: Xác định phản ứng hóa học xảy ra giữa dung dịch và quặng.
- Viết phương trình ion: Viết phương trình ion rút gọn của phản ứng.
- Tính toán nồng độ: Tính toán nồng độ của các ion trong dung dịch.
- Xác định lượng kim loại: Tính toán lượng kim loại được tách ra.
Ví Dụ Giải Bài Tập Điều Chế Kim Loại
Khử 16 gam Fe2O3 bằng CO ở nhiệt độ cao, tính khối lượng Fe thu được?
Phương trình phản ứng: Fe2O3 + 3CO -> 2Fe + 3CO2
Số mol Fe2O3 = 16/160 = 0.1 mol
Theo phương trình, 1 mol Fe2O3 tạo ra 2 mol Fe.
Vậy 0.1 mol Fe2O3 tạo ra 0.2 mol Fe.
Khối lượng Fe thu được = 0.2 * 56 = 11.2 gam
GS. TS. Nguyễn Văn A, chuyên gia hóa học, cho biết: “Việc nắm vững các phương pháp điều chế kim loại là nền tảng quan trọng cho việc học tập và nghiên cứu sâu hơn về hóa học vô cơ.”
Kết Luận
Giải bài tập điều chế kim loại đòi hỏi sự hiểu biết về các phương pháp điều chế và kỹ năng tính toán. Bài viết này đã cung cấp những kiến thức cơ bản và ví dụ minh họa để giúp bạn giải quyết các bài tập một cách hiệu quả. Hi vọng bài viết này sẽ giúp bạn tự tin hơn trong việc giải bài tập điều chế kim loại. Xem thêm phương pháp giải bài tập dãy điện hóa kim loại.
FAQ
- Phương pháp nhiệt luyện thường dùng cho kim loại nào?
- Thủy luyện là gì?
- Điện phân được sử dụng để điều chế kim loại nào?
- Làm thế nào để tính khối lượng kim loại thu được trong phản ứng nhiệt luyện?
- Tại sao cần phải cân bằng phương trình phản ứng?
- Có những yếu tố nào ảnh hưởng đến hiệu suất điều chế kim loại?
- Ứng dụng của điều chế kim loại trong đời sống là gì?
Mô tả các tình huống thường gặp câu hỏi
Học sinh thường gặp khó khăn trong việc xác định phương pháp điều chế phù hợp với từng loại quặng, cũng như tính toán hiệu suất phản ứng.
Gợi ý các câu hỏi khác, bài viết khác có trong web.
Bạn có thể tìm hiểu thêm về giải hóa 12 bài 25 và giải bài tập lí 9 bài 10.